搜索

对映体识别在有机化学,药物化学,材料化学和生命科学的发展中有着至关重要的作用。近日,朱亮亮研究团队提出一种用于广泛识别手性对映体的超分子凝胶策略,通过分子间手性传递以及嵌段共聚物微相分离的协同作用从结构层面而非化学层面来扩大手性对映体的识别,并通过超分子凝胶的塌陷使手性识别具有肉眼可视性(Fig. 1)。
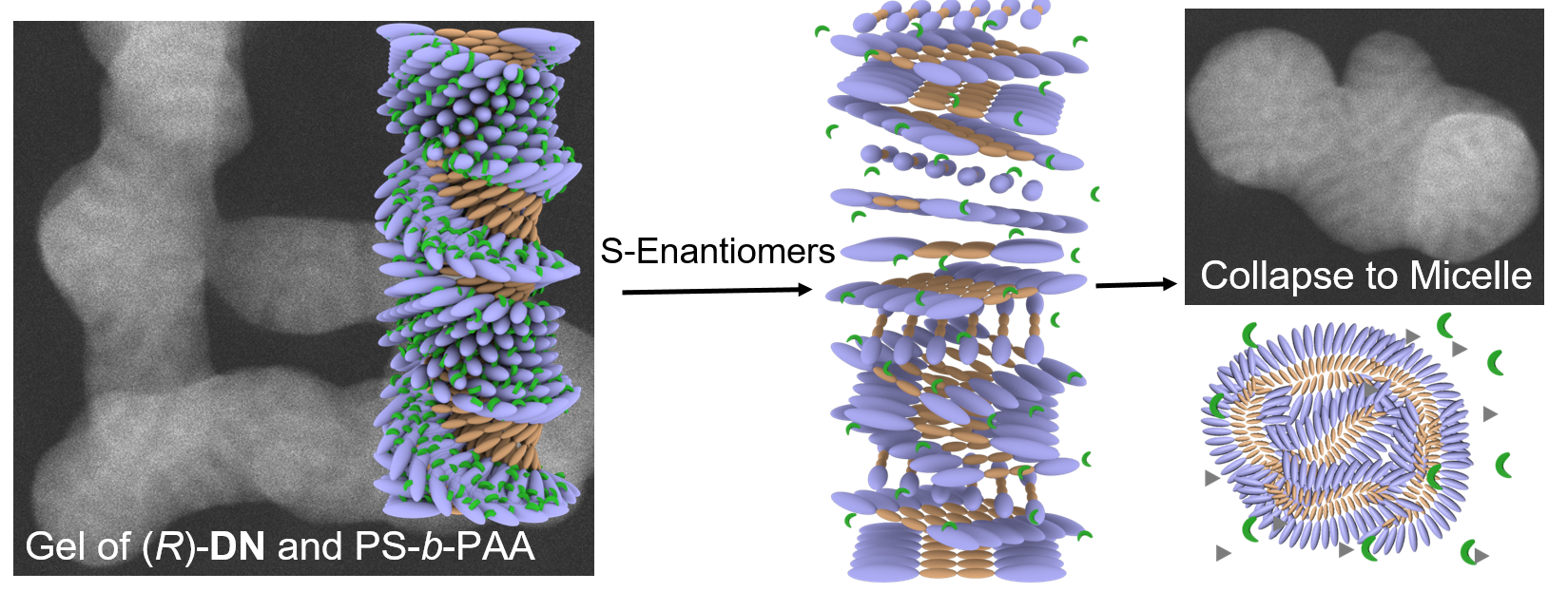
Fig. 1 共组装超分子手性结构以及对映体识别凝胶-胶束变化
仿照自然界中的手性结构,人工手性体系在手性传感器,不对称催化,手性光电器件,对映体分化等方面发挥重要的作用。对映分化通常依赖于手性材料与引入的立体异构体之间的某些立体选择性相互作用,因此当前的人工手性体系通常仅对一种或几种手性异构体具有特定的对映选择性。一些研究者利用对映体分子与手性凝胶因子特定的不对称取代反应构筑可视的手性拆分凝胶结构(J. Am. Chem. Soc., 2010, 132, 7297;Adv. Mater., 2013, 25, 5304, etc.),然而通过单一材料设计来感测一系列手性物种的单一对映异构体是一项巨大的挑战。
面对这一挑战,朱亮亮团队设计出分层共组装体系以充分放大有机凝胶与对映体结构的立体选择性相互作用。他们将具有轴手性的分子“连接器”—带有咪唑基修饰的联萘基衍生物(R)-DN通过氢键作用与非手性嵌段共聚物PS-b-PAA在乙醇中发生共组装,手性传递作用诱导形成具有相分离结构的扭曲纳米纤维。嵌段共聚物的微相分离结构有效的将联萘基团分隔开来,使超分子结构具有荧光增强、圆二色信号(CD)和圆偏振发光(CPL)放大效应(Fig. 2)
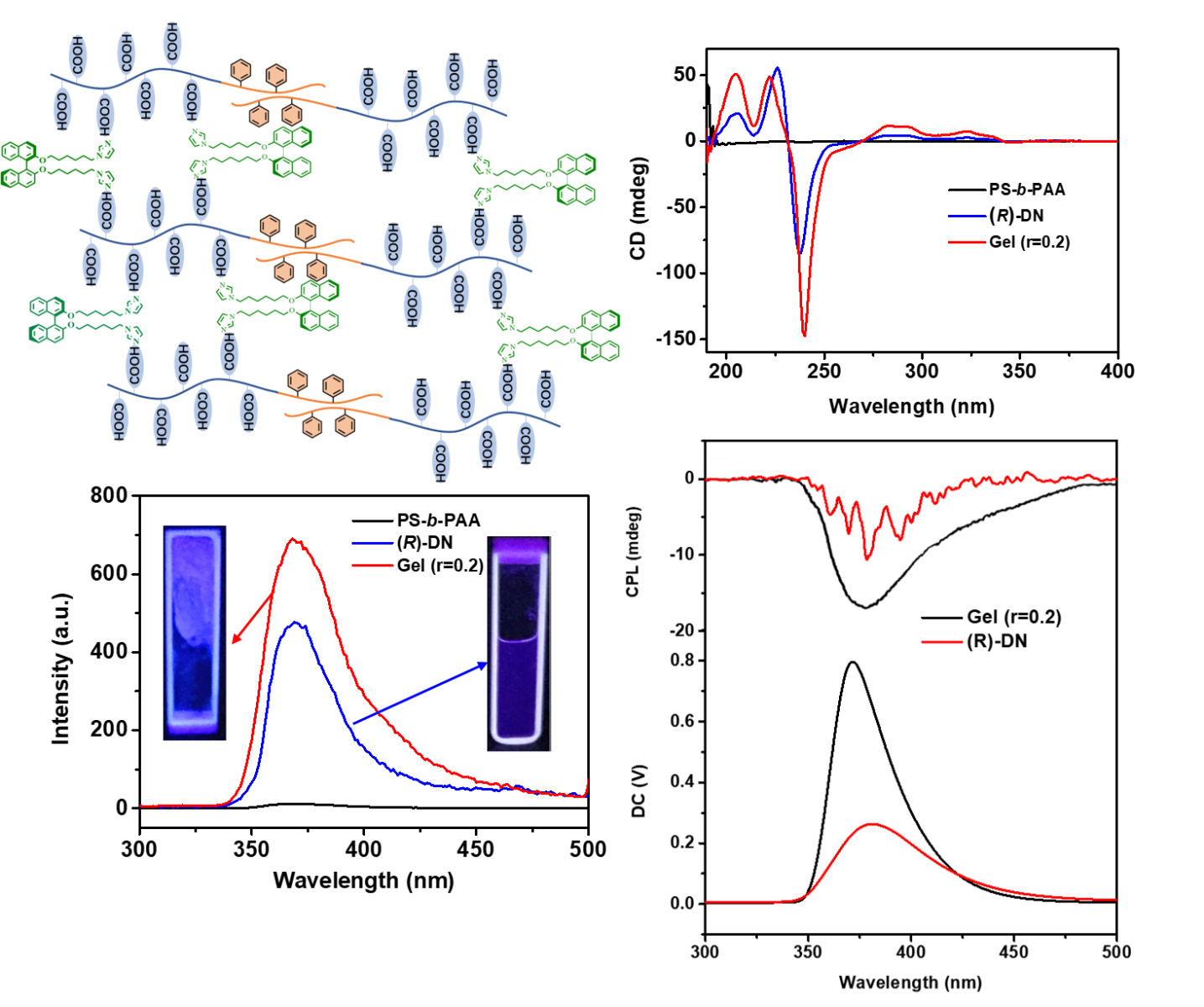
Fig. 2 超分子共组装体系以及有机凝胶放大的光学信号特性
在这样的超分子结构中,手性“连接器”充当凝胶的交联纳米纤维中的支架,使凝胶具有高度的对映体敏感性,在加入一系列微量的(S)-对映体(原子手性、轴手性、点手性、手性聚合物等)后凝胶发生塌陷,扭曲纤维结构转变为胶束状,并伴随着凝胶荧光发射猝灭和CPL信号的削弱(Fig. 3)。
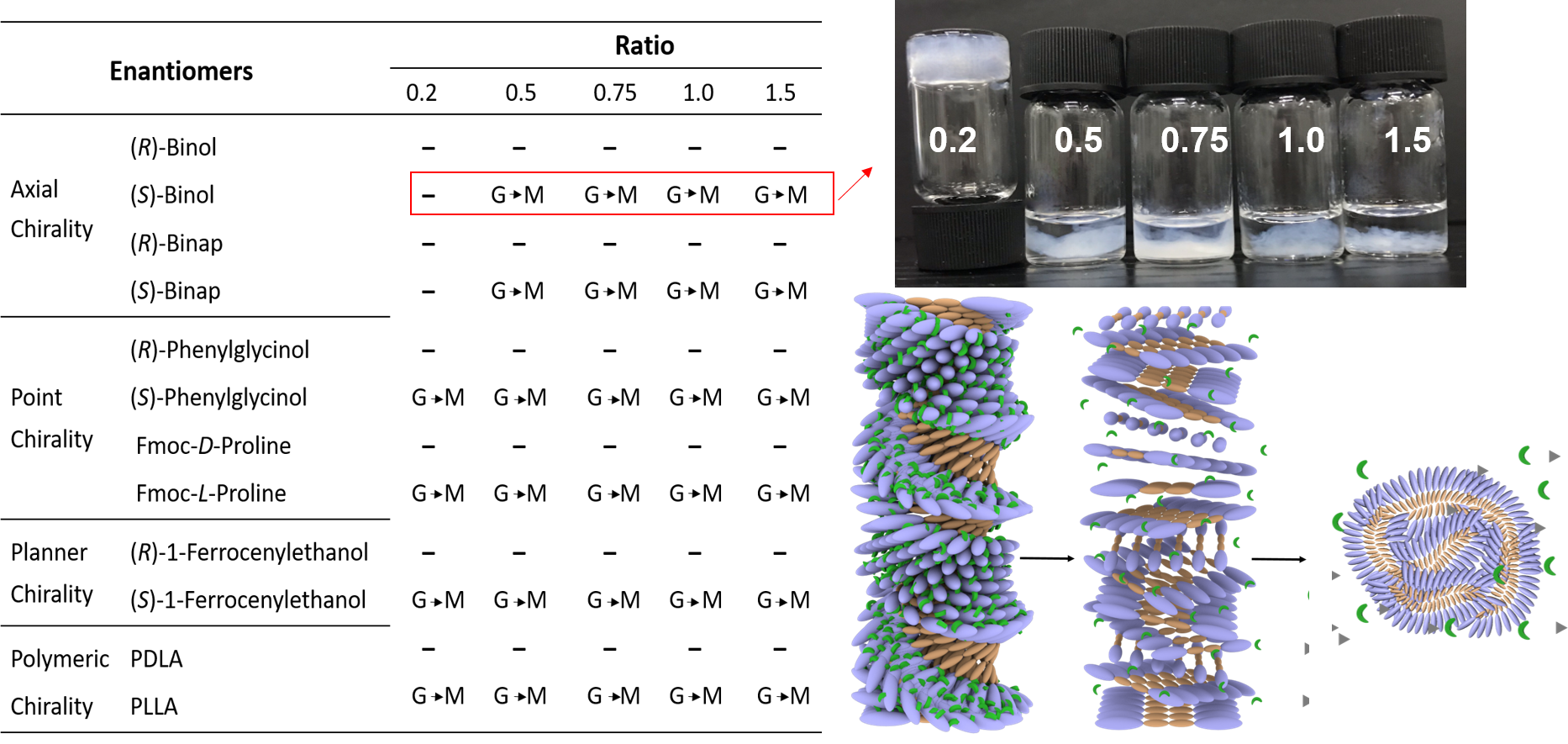
Fig. 3 超分子凝胶在对映体识别的“可视化”
这项工作将手性结构传递与嵌段共聚物微相分离相结合,构筑出对不对称手性分子具有高敏感性立体选择性相互作用的超分子凝胶体系,为对映异构体的可视化识别提供了一种简单有效且适用范围广的手段。
相关成果以“Chirality Transfer in Co-Assembled Organogels Enabling Wide-Range Naked-Eye Enantiodifferentiation” 近日发表在ACS Nano上 (DOI: 10.1021/acsnano.9b06250)。该工作的第一作者是岳兵兵博士,于复旦大学毕业后在上海理工大学任教。
全文链接:
https://pubs.acs.org/doi/full/10.1021/acsnano.9b06250
朱亮亮课题组主要致力于在超分子组装的基础上探索和构建先进的动态调控体系,围绕分子发光能级和手性调控等问题,运用多学科手段将不同的刺激响应行为与超分子共组装手段结合,以促进超分子纳米结构在多色发光转换、高灵敏度光学检测、选择性成像和生物治疗等前沿领域的应用,目前在Proc. Natl. Acad. Sci. USA., Nat. Commun., J. Am. Chem. Soc., Angew. Chem. Int. Ed., Chem. Sci. 等期刊发表多篇高水平论文(更多信息参见朱亮亮课题组网站:http://zll.fudan.edu.cn/)。




