搜索

近日,杨武利教授课题组提出了利用光热效应释放一氧化氮(NO)气体分子用于耐药型肿瘤治疗的新策略。通过将具有良好光热效果的纳米载体和热敏感的NO供体结合,构建了一种新型NO纳米发生器,实现了近红外光照射下精准可控的NO释放,再结合靶向分子,该纳米平台可有效靶向肿瘤部位同时逆转肿瘤的多药耐药性,从而增强化疗效果,为耐药型肿瘤的治疗提供了新途径,对NO相关的疾病治疗也具有重要意义。该工作最近发表在《先进功能材料》(Advanced Functional Materials)上,详见:Ranran Guo, Ye Tian, Yajun Wang, and Wuli Yang*. Near-infrared Laser-Triggered Nitric Oxide Nanogenerators for the Reversal of Multidrug Resistance in Cancer. Advanced Functional Materials, 2017, 27, 1606398.
一氧化氮(NO)是人体内重要的气体信号分子,它在血管平滑肌舒张,血小板黏附,炎症和免疫反应,神经传递等多种生命活动中发挥着重要作用。近年来,利用NO这类气体分子治疗相关疾病被认为是一种新型的治疗手段,具有广阔的应用前景,然而,如何实现NO分子在体内的运输以及准确的控制释放仍然是一个巨大的难题。
为了解决这一问题,杨武利教授团队构建了独特的近红外光响应的NO纳米发生器。利用光热试剂和热敏感NO供体结合,在808 nm的近红外光照射下,该纳米平台可以将光能有效转化为热能,从而促进热敏感的供体释放NO(图 1)。
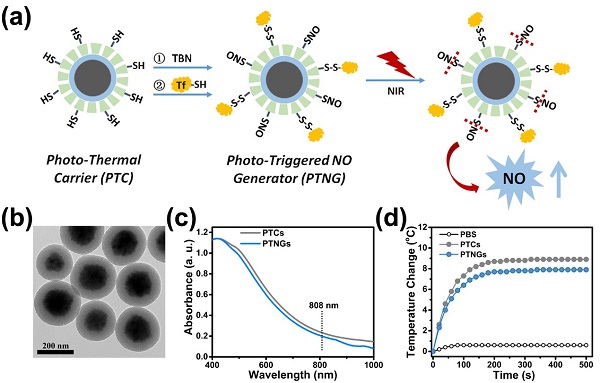
图1. NO纳米发生器的构建示意图
他们在研究过程中发现, NO的释放过程对近红外光具有良好的响应,在体外表现出明显的off/on行为,并利用激光共聚焦进一步在细胞水平上验证了NO响应释放的能力(图2);之后他们将该NO释放平台用于耐药型癌症的治疗。细胞实验结果表明产生的NO分子能够抑制耐药型癌细胞的P型糖蛋白表达,从而有效提高细胞内化疗药物的富集,增强杀伤效果;在耐药型肿瘤模型的裸鼠实验中,这一结果被再次证实,实验组的肿瘤生长得到了有效控制。这种近红外光响应释放NO的纳米平台对于耐药型肿瘤和其它NO相关疾病的治疗具有重要意义。
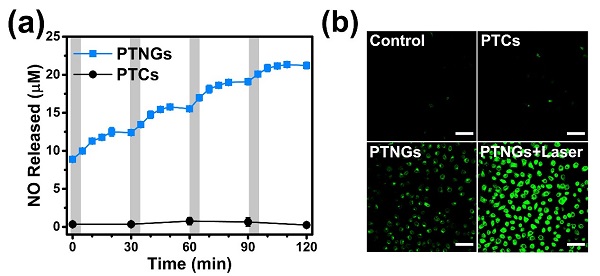
图2. NO的释放检测: (a) 近红外光照射下(808 nm, 0.3 W·cm-2, 5 min), NO释放的off/on行为;(b) 利用荧光探针DAFDA检测细胞内NO产生的激光共聚焦图像。




