搜索

提升纳米粒子对生物信号的响应灵敏度是增强响应聚合物在生物医学领域“对症下药”应用的关键科学问题。目前已广泛开发了侧基响应型和主链响应型两种聚合物响应模式,能够实现对生物体内生物信号的“1-to-1”响应和“1-to-N”响应。然而,这两种响应模式的临界响应阈值处在CT = 10-3~10-6 mol/L的范围内,难以匹配细胞环境中大多数生物信号的痕量浓度(10-6~10-9 mol/L)。这一棘手问题限制了响应性聚合物材料在细胞中的实际生物应用。
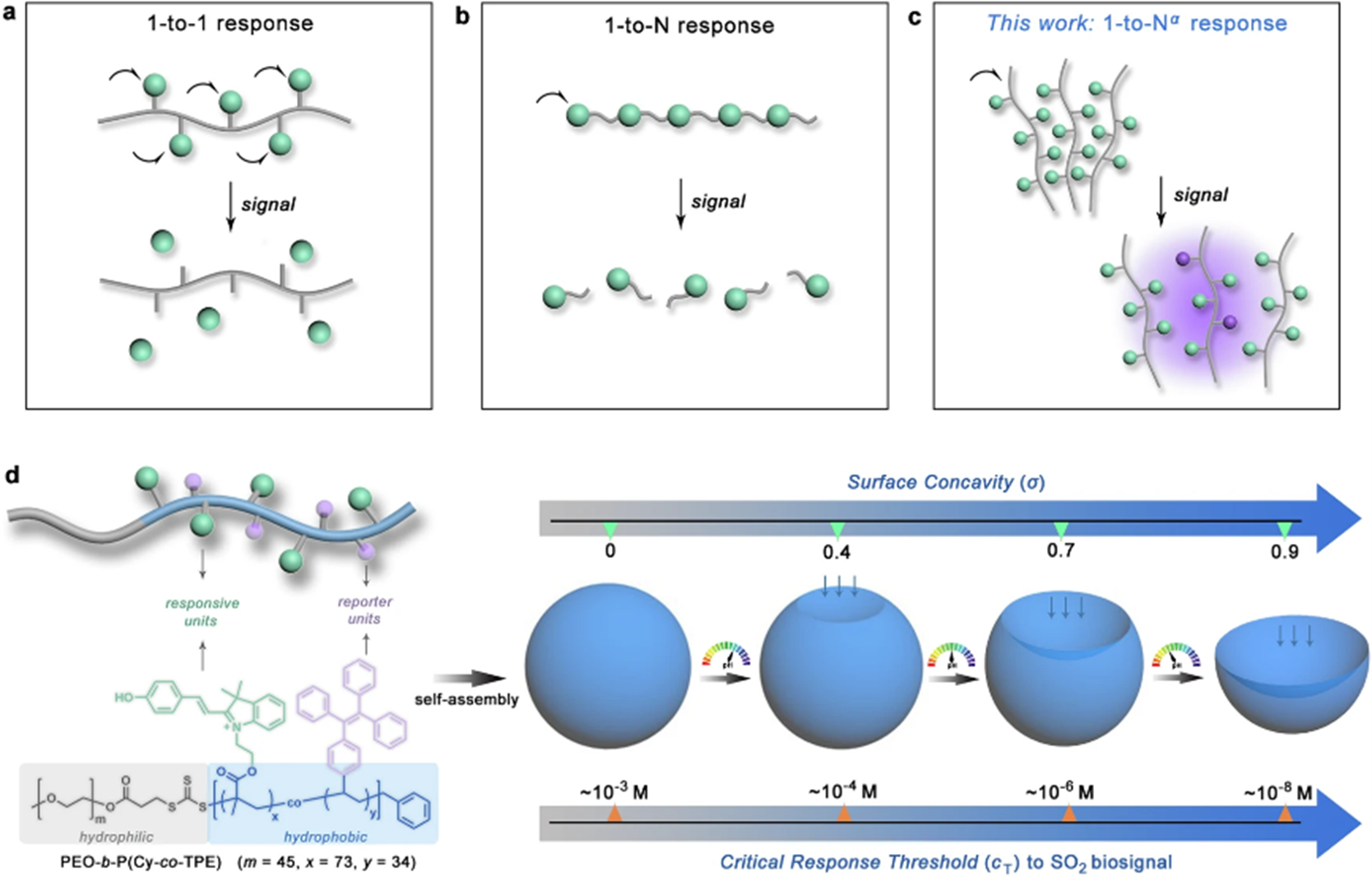
图1. (a-c) 聚合物的传统信号响应模式(1-to-1和1-to-N);(d) 通过调节纳米碗膜凹陷度实现对生物信号的非线性响应模式(1-to-Nα)
为克服该领域长期存在的这一瓶颈,复旦大学高分子科学系闫强课题组发展了一类聚合物非球形囊泡组装系统,通过精确控制碗形囊泡的膜凹度(σ),实现了对生物信号“1-to-Nα”的指数型非线性放大效应,并以此构建了能够对生物痕量SO2气体信号进行超灵敏检测的纳米平台,聚合物对SO2生物信号的临界响应阈值CT可提高5个数量级,达到10-8~10-9 mol/L水平(图1)。
2024年10月2日,该成果以《纳米碗表面凹度对生物信号临界响应阈值的非线性放大效应》(Nonlinear amplification of nanobowl surface concavity on the critical response threshold to biosignals)为题发表于《自然·通讯》(Nature Communications)。
课题组采用冷冻电镜等微观可视化表征方法,跟踪了聚合物囊泡随pH的形貌演变,证实了囊泡膜在pH由8.3降至5.5时,组装体可光滑球形逐渐变形为单一位点凹陷的碗形囊泡,且膜凹度σ可从0提高到0.9。这种变形机制主要是由于组装体内聚合物链间的氢键相互作用和基团间π-π相互作用增强,导致链内聚力提高的结果。
进而,研究发现了纳米碗的凹度与其对SO2信号分子响应能力之间的关系:无凹陷的纳米球仅能实现“1-to-1”响应;而具有深凹陷的纳米碗会由于具有更高的聚集诱导发光基元的堆积密度而对SO2呈现高度敏感,其临界响应阈值可提高至纳摩尔级别,与细胞内真实SO2气体信号的浓度相匹配,从而证实了聚合物纳米粒子的形态可以非线性影响其响应能力的结论(图3)。这项研究首次证明聚合物自组装体内链的聚集状态与其功能之间存在至关重要的依赖关系,成功构筑了第一例能对SO2生物信号实现1到Nα响应的新型聚集诱导发光材料,为在痕量水平上原位检测其他生物信号提供粒子形状选择上的技术指导,为开发更多高性能的智能检测器提供了新的构建思路。
复旦大学高分子科学系、聚合物分子工程国家重点实验室为论文唯一单位;复旦大学高分子系博士生李雪凤为第一作者;复旦大学闫强教授为通讯作者。研究工作得到了国家自然科学基金的支持。
论文链接:
https://doi.org/10.1038/s41467-024-53053-3




