搜索

细胞焦亡是由Gasdmine (GSDM)家族介导的高度促炎的细胞程序性坏死。细胞焦亡不仅规避了凋亡抵抗,还能够产生损伤相关分子模式(DAMPs)和促炎细胞因子,触发肿瘤特异性免疫。光焦亡(光触发焦亡)是光动力疗法(PDT)的一个新兴研究分支,通过光焦亡重塑肿瘤免疫微环境是一种很有前景的癌症治疗方法。然而,目前已知可以诱导光焦亡的光敏剂不仅非常匮乏,而且大多数这类光敏剂都是偶然发现的。简而言之,缺乏一种系统性的光敏剂分子结构的通用设计原理以指导高效光焦亡的发生。
鉴于此,复旦大学高分子科学系朱亮亮教授和杨武利教授联合上海交通大学上海儿童医学中心烧伤整复外科朱世辉教授等团队合作发展了一种光焦亡光敏剂分子结构的通用设计策略——即让一个光敏母核被多个阳离子端基(例如用于线粒体靶向的吡啶鎓/咪唑鎓端基)包夹的分子结构模型。通过该策略能够实现一系列光敏剂的合成与制备,使其仅需10s(0.4 J/cm2)光照即可实现高效光焦亡,从而可用于高抑制效率的肿瘤免疫治疗。
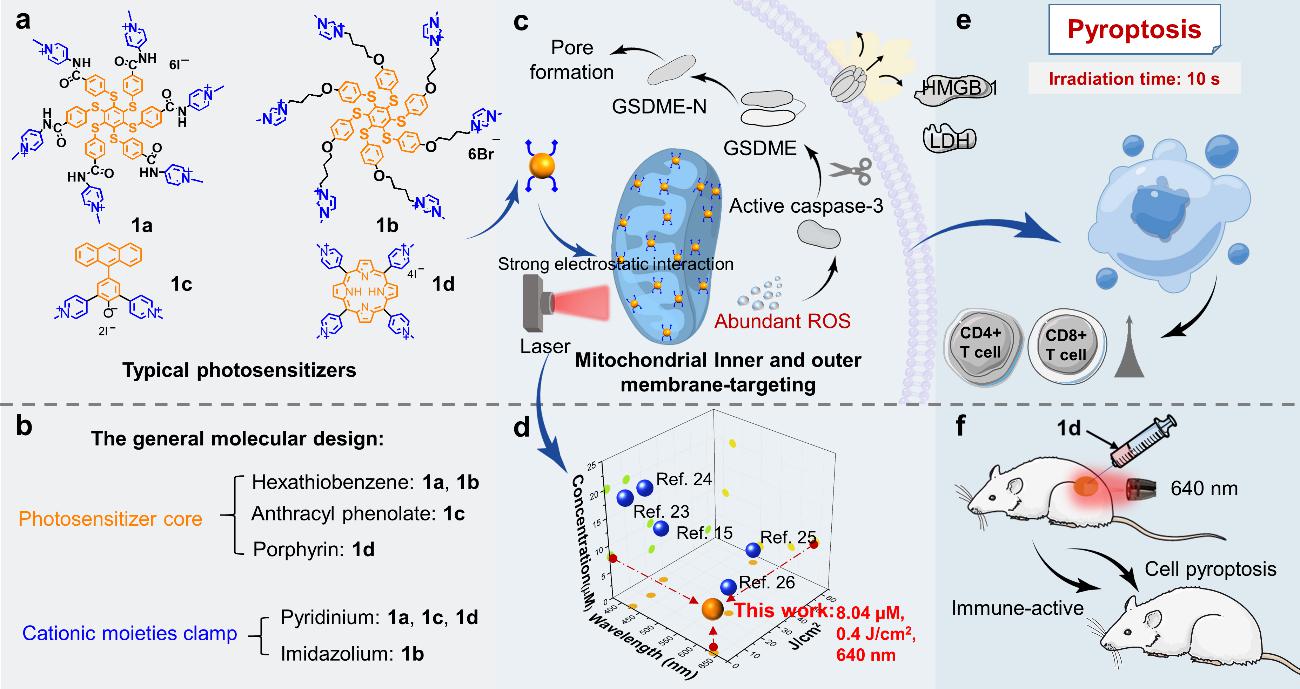
图1.研究概要
在本研究中,作者提出了光敏剂通过强静电相互作用实现强烈的线粒体靶向能力至关重要,因此合成了吸收波长从紫外区到近红外区4种光敏剂和4个对照光敏剂,目标光敏剂可以通过强烈的线粒体靶向诱导细胞光焦亡,对照光敏剂均未观察到细胞焦亡现象。静电结合能力导致的强线粒体靶向能力、以及光敏剂在光照下产生ROS的量子产率的综合因素导致了高效细胞光焦亡能力。
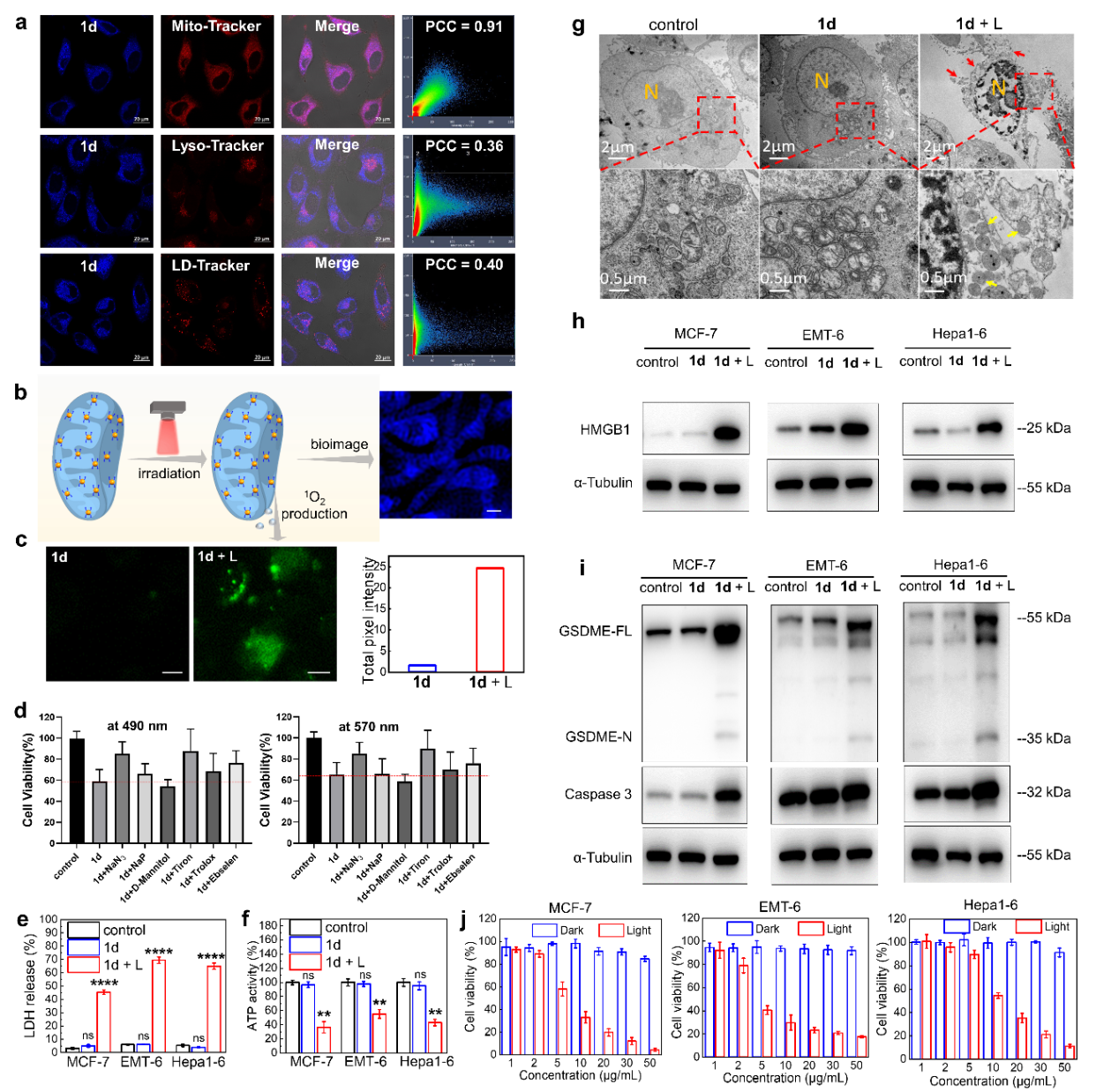
图2.光焦亡机理探究
作者通过详细研究代表性光敏剂1d在细胞器靶向能力,活性氧类型,线粒体形貌变化以及细胞焦亡相关通路等方面,证实了光敏剂是通过靶向并损伤线粒体,引起Caspase-3/GSDME介导的细胞光焦亡。
作者通过控制光照时间和光照功率,发现光敏剂1d仅需光照10s即可诱导细胞焦亡,这种高效的光焦亡能力也证实了该通用策略的有效性。
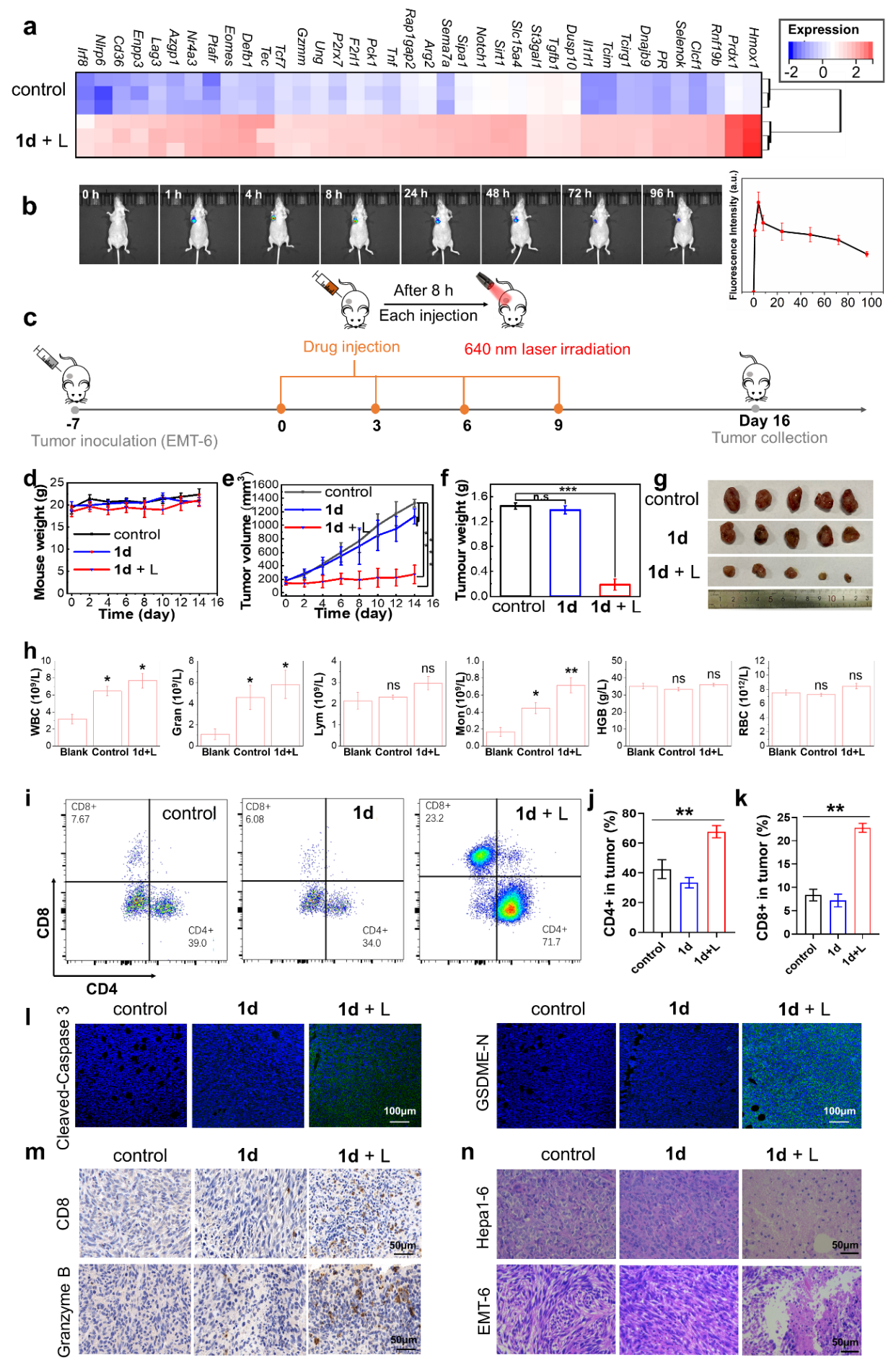
图3:在体的免疫效应和免疫治疗
最后作者通过动物实验进一步验证了光焦亡触发了明显的全身免疫响应。
综上所述,该工作开发了一种通用的分子结构设计原理,用于制备能够实现高效光焦亡的光敏剂。其理念是通过光敏剂结构因素,让一个光敏母核被多个阳离子端基(例如用于线粒体靶向的吡啶鎓/咪唑鎓端基)包夹的分子结构模型。使其产生与线粒体强静电相互作用,实现线粒体的强烈靶向,并通过光生ROS损伤线粒体,引起Caspase-3/GSDME介导的细胞焦亡,最终触发明显的全身免疫响应。该结构范式对于具有光焦亡能力的光敏剂开发(尤其是针对线粒体的 PDT)提供了指导性思路。
相关研究成果以题为“A General Molecular Structural Design for Highly Efficient Photopyroptosis that can be Activated within 10 s Irradiation”在线发表于《Advanced Materials》上。复旦大学高分子科学系原博士生刘青松、姚先先和周璐璐(现分别在海军军医大学第一附属医院、益杰立科生物科技有限公司、清华附中嘉兴实验高级中学任职)承担了本文的主要工作。
原文链接:https://onlinelibrary.wiley.com/doi/epdf/10.1002/adma.202401145




